- TRSET
Element molekülü ve Apolar Kovalent Bağ arasındaki bağlantı.
Polar Kovalent Bağ ve Apolar Kovalent Bağ arasındaki farklar.
Kovalent Bağlar ve atom yörüngesine ilk adım #Kimya #Polar #Apolar
+ index service
+ TR Search Engine Technology
Kovalent Bağ
İki atom arasında bir veya daha fazla elektronun paylaşılmasıyla karakterize edilen kimyasal bağa verilen addır. Genellikle bağ tanımı; ortaya çıkan molekülü bir arada tutan ortak çekim gücü olarak nitelendirilir. Paylaşılan elektron veya elektronlar, her iki çekirdek etrafında dolaşırlar. İki çekirdek arasında kalan bölgede daha uzun süre bulundukları için bu bölgede (-) yüklü bir alan oluşturacaklardır. Bu oluşan alan, her iki çekirdeğe bir çekme kuvveti uygulayarak bir bağ kurmuş olur.
Kovalent bağ, bahsi geçen atomların dış yörüngelerinin dolması ile oluşur. Bu tür bağlar, moleküller arası hidrojen bağından daima daha güçlü, iyonik bağ ile ise ya aynı güçte ya da daha güçlüdür.
Hidrojen (H), amonyak(NH3), klor(Cl), su(H2O) ve azot(N) gibi bazı inorganik maddelerin molekülleri ile tüm organik maddelerin molekülleri kovalent bağ ile bir arada tutulabilir.
Kovalent bağ ; iyonik ve metalik bağın tersine yönlüdür. Yani bağ açılarının etkileşim gücü üzerinde etkisi büyüktür. Bu etkinin kaynağı, kovalent bağların, atomik yörüngelerin üst üste binmesiyle oluşmasından ileri gelir. Atomik yörüngeler (p, d, ve f orbitalleri) hepsi yönlü karakterde olup, bağlanma esnasında önemli ölçüde yöne bağlı etkileşime neden olurlar.
Kovalent bağ, genellikle benzer elektronegatifliğe sahip atomlar arasında gerçekleşir. Bu nedenle ametaller, daha kolaylıkla kovalent bağı tercih eder ve metaller de kolayca yerlerinden oynatılabilen elektronların daha serbestçe dolaşabildiği metalik bağ yaparlar. Ametallerde bir elektronun serbest kalması daha zordur, dolayısıyla benzer elektronegatifliğe sahip bir madde ile birleşme söz konusu olduğunda o elektronun paylaşılması tek seçenek haline gelir.
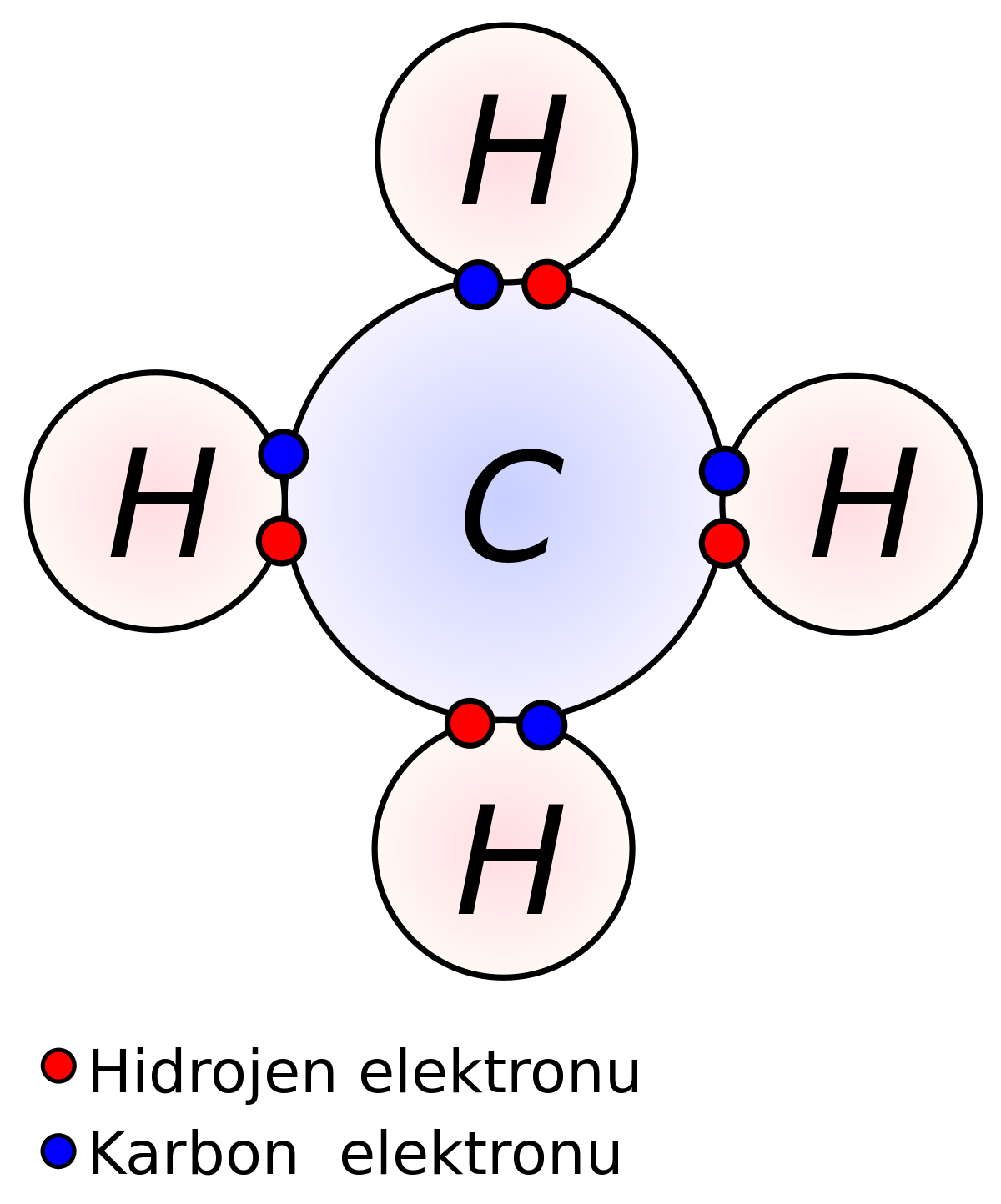
Kovalent bağ, Polar Kovalent Bağ ve Apolar Kovalent Bağ olmak üzere ikiye ayrılır.
Polar Kovalent Bağ
Farklı ametaller arasında oluşan bağa polar kovalent, yani kutuplu bağ denir. Elektronlar iki atom arasında eşit olarak paylaşılmadığından kutuplaşma gerçekleşir ve bu duruma polar kovalent bağ adı verilir. Örnek olarak Hidrojen florür (HF) bileşiğinde Hidrojen ve Flor atomları elektron ortaklığı ile polar kovalent bağ yapar.
Apolar Kovalent Bağ
Aynı cins iki ametal atom arasında meydana gelen kovalent bağdır ve bu şekilde meydana gelen moleküllere element molekülü adı verilir. Ortaklaşa kullanılan elektronlar ise her iki atom çekirdeği tarafından eşit oranda çekilir. Bunun sebebi çekirdek yüklerinin aynı olmasıdır.
Video : Esra ATEŞ
Ağlarsa anam ağlar, gerisi kovalent bağlar









 Bu Sayfayı Paylaş
Bu Sayfayı Paylaş WhatsApp CH
WhatsApp CH Twitter
Twitter YouTube
YouTube Linked in
Linked in Instagram
Instagram Facebook
Facebook Türkçe
Türkçe Deutsch
Deutsch English
English